Neuigkeiten zur Erforschung von Medizinprodukte-Eigenherstellungen
Leipzig, 24.02.2026
Im letzten halben Jahr hat sich im Bereich der Regulatorik für Medizinprodukt-Eigenherstellungen einiges getan – und es gibt gute Nachrichten! Dieser regulatorische Rahmen betrifft die meisten CDS-Entwicklungen an universitären Standorten. Besonders erfreulich ist, dass das Eigenherstellungs-Privileg bis Ende 2025 deutlich an Bedeutung gewonnen hat.
Medizinprodukt-Eigenherstellungen können ohne Regulierung durch MDR oder IVDR erforscht werden
Die neue Mitteilung der MDCG (2025-5) räumt mit einem weit verbeiteten Missverständnis von Rechtsgutachten und Ethikkommissionen zu Medizinprodukt-Eigenherstellungen auf, die Studien damit immer in den Rechtsrahmen der MDR („klinische Prüfung“) oder IVDR („klinische Leistungsstudie“) gesetzt haben.
Nun ist klar: Ist eine fertige Eigenherstellung vorhanden und erfüllt sie sämtliche Voraussetzungen von Art. 5(5) einschl. Anhang I, entfällt die weitere Regulierung dieser Studien im Rahmen der IVDR (Artikel 57 und 58), solange die Leistungsstudie Im Rahmen der Zweckbestimmung vorgenommen wird. Dass diese Einordnung auch auf Eigenherstellungen im Rahmen der MDR zu übertragen ist, versicherte uns Rechtsanwalt Prof. Gassner (u.a. Herausgeber des gerade erschienenen Standardwerks „Medizinprodukterecht“, ISBN: 978-3-8487-7622-1) in persönlicher Korrespondenz.
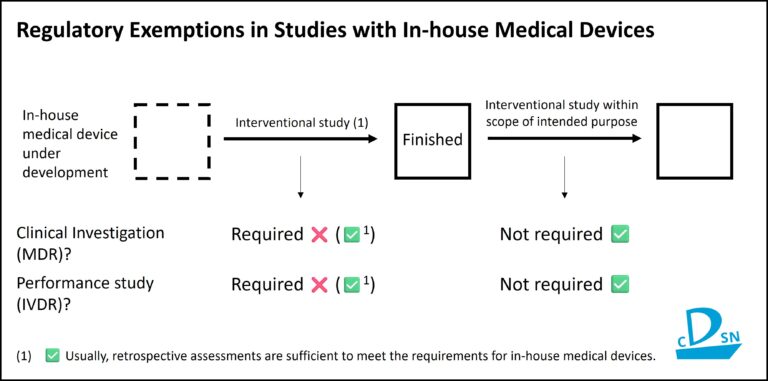
Anders ausgedrückt: Wird eine „fertige“ Eigenherstellung, für die bereits ausreichende Leistungsdaten z.B. im Rahmen einer retrospektiven klinischen Bewertung vorhanden sind, weitergehend im Rahmen ihrer Zweckbestimmung untersucht, entfällt der Rechtsrahmen der MDR oder IVDR. Das sind tolle Neuigkeiten für alle, die prospektive und interventionelle Studien planen!
AI Act: Medizinprodukt-Eigenherstellungen sollen nicht als Hochrisiko KI-System eingestuft werden.
Auch wenn der Zusatzaufwand von einer Medizinprodukt-Eigenherstellung bei Einstufung als Hochrisiko KI-Systems durch den AI Act verhältnismäßig gering erscheint, ist dies doch eine erfreuliche Nachricht an alle Unikliniken, die dabei sind entsprechende Eigenherstellungen zu entwickeln. Auch diese Nachricht beruht auf einer Mitteilung der MDCG (2025-6).
Neue MDR-Gesetzesvorschläge der EU-Kommission: Zukünftig können Eigenherstellungen an andere Gesundheitseinrichtungen abgegeben werden.
Kurz vor Weihnachten und nach dem Einholen eines EU-weiten Feedbacks zur aktuellen MDR (an dem auch einige CDSN-Mitglieder mitgearbeitet haben) wurden die neuen Gesetzesvorschläge der EU-Kommission veröffentlicht. Darin wird die Entwicklung und Erforschung in multizentrischen Settings, so wie die Planungssicherheit bei Eigenherstellungen deutlich gestärkt. Zukünftig soll es eine Übergangszeit von 10 Jahren geben, falls ein gleichwertiges CE-zertifiziertes Produkt auf den Markt kommt. Zudem sollen Eigenherstellungen an andere Gesundheitseinrichtungen abgegeben werden können, so dies im Interesse der Patientensicherheit oder der öffentlichen Gesundheit dient. Ein Umstand, der sicherlich auf die meisten CDSN-assoziierten Projekte zutrifft!
Was denken Sie dazu? Schreiben Sie uns, wenn Sie an einem Austausch interessiert sind.
